ADPKD: DIAGNOSI E TERAPIA
CRITERI DIAGNOSTICI DI ADPKD ALL’ECOGRAFIA
Età 15-29 ≥3 cisti (0 cisti criterio di esclusione)
Età 30-39 ≥3 cisti (0 cisti criterio di esclusione)
Età 40-59 ≥2 cisti in ogni rene (0 cisti criterio di esclusione)
CRITERI DIAGNOSTICI DI ADPKD ALLA RMN
Età 16-40 >10 cisti (<5 criterio di esclusione)
CARATTERISTICHE CLINICHE DI ADPKD
Difetto di concentrazione delle urine
Ematuria
Ipertensione arteriosa
Insufficienza renale
Dolore da ingombro
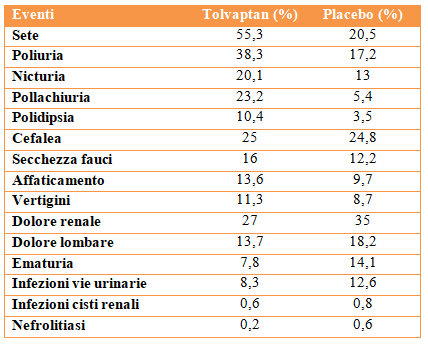
CRITERI DI PRESCRIZIONE DEL TOLVAPTAN
1. 30-40 anni con eGFR 45-90 mL/min 1.73 m² in progressione
2. 40-50 anni con eGFR 45-60mL/min 1.73 m² in progressione
Non epatopatici, gravidanza, allattamento, bambini, disionie del sodio, allergici all’amido di mais.
Raccomandazione 1
Si suggerisce di prescrivere tolvaptan a pazienti adulti con ADPKD di età <50 anni con CKD in stadi 1–3a (eGFR >45 mL/min 1.73 m²) che abbiano malattia in rapida progressione dimostrata o probabile, ma di interpretare lo stadio della CKD in combinazione con l’età.
Raccomandazione 2
Si raccomanda di non iniziare tolvaptan in pazienti di età 30–40 anni con CKD in stadio 1 (eGFR >90 mL/min 1.73 m²).
Raccomandazione 3
Si raccomanda di non iniziare tolvaptan in pazienti di età 40–50 anni con CKD in stadio 1 o 2 (eGFR >60 mL/min 1.73 m²).
Rapida progressione
Un declino annuale confermato dell’eGFR ≥5 mL/min 1.73 m² in 1 anno,
e/o ≥2.5 mL min/1.73 m² per anno in un periodo di 5 anni, definisce la progressione rapida.
Il principale fattore di progressione rilevato nella malattia policistica è il volume renale.
TOLVAPTAN IN ADPKD: CONTROINDICAZIONI E RELATIVE CAUSE
| CONTROINDICAZIONE | CAUSA DELLA CONTROINDICAZIONE |
|---|---|
| malattia renale cronica stadio 5 (GFR misurata o stimata < 15 mL/min 1.73 m²) |
dati mancanti e sospetto di danni epatici più frequenti |
| trattamento dialitico cronico | dati mancanti e sospetto di danni epatici più frequenti |
| assenza o riduzione del senso di sete | rischio elevato di disidratazione |
| ipovolemia, ipersodiemia, ipo- e pseudo-iposodiemia (iperglicemia severa) |
rischio elevato di peggioramento squilibrio idro-elettrolitico |
| danno epatico severo (ipertransaminasemia >3xlsn o iperbilirubinemia >2xlsn) |
rischio elevato di peggioramento del danno epatico |
| ipersensibilità o reazioni anafilattiche a tolvaptan o eccipienti (amido di mais, idrossipropilcellulosa, lattosio, stearato di magnesio, cellulosa microcristallina, indigo carminio, alluminio) |
rischio elevato di reazioni allergiche |
| disordini metabolismo di lattosio o galattosio | rischio di tossicità (lattosio negli eccipienti) |
| Gravidanza | dati assenti |
| Allattamento | dati assenti |
| età pediatrica | dati assenti |
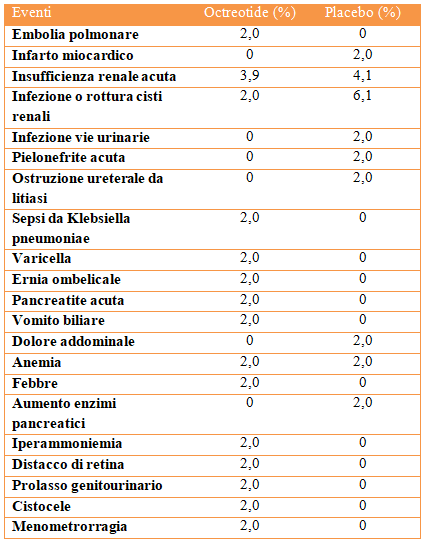
CRITERI DI PRESCRIZIONE DELL’OCREOTIDE
Età >18 anni
Diagnosi clinica e strumentale di ADPKD
eGFR (MDRD4) ≥15 ml/min 1.73 m2 e <30 ml/min 1.73 m2
Criteri di esclusione: gravidanza e allattamento, inadeguata contraccezione in donne in età fertile.
Il piano terapeutico prevede l’iniezione IM profonda in sede glutea per lato di una fiala di 20 mg di Octreotide a lunga durata di azione ogni 28 giorni, per una dose totale di 40 mg ogni 28 giorni.
Malattia di Fabry
Genetica: X linked (gene GLA)
Biochimica: danno lisosomiale (attività dell’enzima a-Gal A), accumulo di GL3 nelle cellule.
Clinica: dolore neuropatico, aritmie cardiache, insufficienza cardiaca, IVS, ictus, TIA, lesioni della sostanza bianca, insufficienza renale, proteinuria, diarrea, dolore addominale, angiocheratoma, acroparestesia, ipoidrosi/anidrosi, opacità corneale, opacità lenticolare (cataratta anteriore o posteriore subcapsulare), tortuosità vascolari retiniche, acufeni.
Nefropatia: iniziale espansione mesangiale e iperfiltrazione glomerulare, disfunzione e perdita dei podociti, alterazione della membrana basale glomerulare, glomerulosclerosi. All’esame urine cellule epiteliali con vacuoli pieni di glicosfingolipidi, “Croci di Malta”. Diffusi depositi di glicolipidi. Patologia multicistica renale
Cardiopatia: ECG= PR breve, IVS marcata (concentrica), profonda depressione ST, inversione dell’onda T.
Diagnosi genetica: nel maschio dimostrazione del difetto dell’attività dell’enzima a-Gal A nel plasma o nei leucociti, nella femmina identificazione della mutazione o evidenza di Gb3 a livello tissutale. Il test enzimatico, il dosaggio dei biomarcatori e la genetica possono essere effettuati su una macchia di sangue essiccata su carta da filtro (carta di Guthrie).
Terapia: Per la malattia di Fabry è disponibile la terapia di sostituzione enzimatica (infusioni endovenose da effettuarsi generalmente ogni 14 giorni) e, per i pazienti che presentano alcune specifiche mutazioni genetiche, anche la terapia a somministrazione orale. Monitorare i livelli plasmatici di un metabolita del Gb3 globotriaosilsfingosina (lyso-Gb3), biomarcatori di malattia e marcatori di efficacia della terapia.
Malattia di Dent
Diagnosi
- Proteinuria a basso peso molecolare (5 x beta2-microglobulina, alfa1-microglobulina, catene leggere, retinol binding protein RBP, PTH) PM < 10.000 D.
- Ipercalciuria (>4 mg/Kg 24h oppure > 0.25 calcio/creatinina oppure 250 mg/24h per F, >300 mg 24h per M)
Almeno uno dei seguenti: nefrocalcinosi, calcoli renali, ipofosfatemia, insufficienza renale, aminoaciduria, rachitismo, familiarità.
La malattia di Dent è un disordine funzionale generale del tubulo prossimale dovuto a specifiche cause genetiche e con precise caratteristiche cliniche
a) Ipofosforemia, ipouricemia, acidosi metabolica
con rachitismo, osteomalacia, ritardo nella crescita, debolezza muscolare
b) Glicosuria, aminoaciduria, proteinuria tubulare, ipovolemia
con iperaldosteronismo, ipopotassiemia, polyuria, disidratazione
c) Flogosi interstiziale e glomerulare, fibrosi
con insufficienza renale
d) Aumentata attivazione della vitamina D e ipercalciuria
con nefrocalcinosi, calcolosi renale.
Fenotipo della malattia di Dent
a) Ipofosfatemia nel 100% dei pazienti
b) 1,25 (OH) D normale o al limite superiore anche in CKD avanzata.
c) Ipercalciuria nel 60% <30 anni, 15% <30 anni.
d) PTH normale.
e) Nefrocalcinosi comune nei bambini.
f) Calcolosi renale nel 30% (ossalato di calcio e/o fosfato)
g) Ipopotassiemia nel 50% >18 anni
Terapia della malattia di Dent
1. Sali di fosfato 250-500 mg x 4-5/die (KPHOS, 250 mg P + K 500 mg (13 mEq)= 2 bustine/die o 20-40 mg/Kg die in 4 somministrazioni)
2. Alendronato
3. Citrato di K
4. Tiazidici
5. Antialdosteronici
6. ACE-I/ARB
7. Sodio bicarbonato